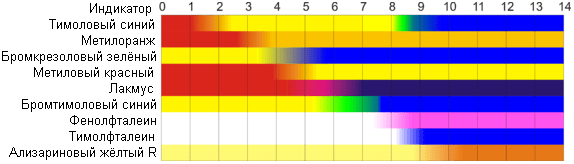
Indicadores naturais de pH
Baixo a influencia dos cambios na reacción do ambiente, non só os compostos utilizados nos laboratorios como indicadores adquiren cores diferentes. Un grupo igualmente numeroso está formado por substancias contidas nos produtos naturais. En varios ensaios, probaremos o comportamento dos indicadores de pH no noso contorno.
Para os experimentos, serán necesarias varias solucións con pH diferente. Pódense obter diluíndo ácido clorhídrico con HCl (a solución de pH 3-4% é 0) e solución de hidróxido de sodio NaOH (a solución ao 4% ten un pH de 14). A auga destilada, que tamén utilizaremos, ten un pH de 7 (neutro). No estudo, utilizaremos zume de remolacha, zume de repolo vermello, zume de arándanos e infusión de té.
En tubos de ensaio con solucións preparadas e auga destilada, botar un pouco de zume de remolacha vermella (foto 1). En solucións ácidas, adquire unha cor vermella intensa, en solucións neutras e alcalinas, a cor tórnase marrón, converténdose nun ton amarelo (foto 2). A última cor é o resultado da descomposición do colorante nun ambiente fortemente alcalino. A substancia responsable da decoloración do zume de remolacha é a betanina. A acidificación do borscht ou da ensalada de remolacha é un "chip" culinario que dá ao prato unha cor apetitosa.
Do mesmo xeito, proba o zume de repolo vermello (foto 3). Nunha solución ácida, o zume vólvese vermello brillante, nunha solución neutra vólvese violeta claro e nunha solución alcalina vólvese verde. Tamén neste caso, a base forte descompón o colorante: o líquido no tubo de ensaio vólvese amarelo (foto 4). As substancias que cambian de cor son as antocianinas. Espolvorear ensalada de repolo con zume de limón dálle un aspecto atractivo.
Outro experimento require zume de arándanos (foto 5). A cor vermella-violeta cambia a vermella nun medio ácido, a verde nun medio alcalino e a amarela nun medio fortemente alcalino (descomposición de colorantes).foto 6). Aquí, tamén, as antocianinas son as encargadas de cambiar a cor do zume.
A infusión de té tamén se pode usar como indicador de pH en solución (foto 7). En presenza de ácidos, a cor vólvese amarela palla, nun medio neutro vólvese marrón claro e nun medio alcalino vólvese marrón escuro (foto 8). Os derivados do tanino son os encargados de cambiar a cor da infusión, dándolle ao té o seu característico sabor agrio. A adición de zume de limón fai que a cor da infusión sexa máis clara.
Tamén paga a pena realizar probas de forma independente con outros indicadores naturais: moitos zumes e decoccións de plantas cambian de cor debido á acidificación ou alcalinización do ambiente.
Mírao no vídeo:
Indicadores naturais de pH
